На протяжении всей истории человечества крупные эпидемии часто сопровождались развитием у переболевших затяжных постинфекционных состояний, выяснила команда международных исследователей во главе с учеными Медицинской школы Йельского университета (США). После коронавирусной пандемии многие столкнулись с так называемым постковидным синдромом. Но на самом деле таких состояний в истории медицины было множество: хронические симптомы после перенесенной инфекции описывались при различных эпидемиях, включая грипп, вирус Эпштейна — Барр, полиомиелит и тяжелый острый респираторный синдром в начале 2000-х. Но, несмотря на явные закономерности, по-прежнему мало известно о том, как возникают постострые инфекционные синдромы. Результаты этой важной аналитической работы опубликованы в журнале Trends in Immunology группы изданий Cell.
Патогены и эпохи разные, паттерн повторяющийся?
Вспышки инфекционных заболеваний всегда приводили к тому, что у некоторых пациентов развивались стойкие, часто необъяснимые симптомы. Эти симптомы очень разнообразны и включают сильную усталость, одышку, нейрокогнитивные и сенсорные нарушения, а также боли в мышцах и суставах. Для многих эти состояния являются крайне изнуряющими, вот только механизмы, их вызывающие, остаются неясными. Выдвигаются разные гипотезы, от персистенции вируса до иммунной дисрегуляции. Но без четкого понимания трудно разрабатывать диагностические и терапевтические подходы.
Постострые симптомы развиваются примерно у 4–20 % детей и 10–20 % взрослых пациентов после перенесенной инфекции SARS-CoV-2. Уже доказано, что постковид связан с дисрегуляцией как врожденного, так и адаптивного иммунитета.
И хотя постковид — относительно новое клиническое явление, постострые постинфекционные синдромы (PAIS) документально фиксируются врачами уже как минимум более века. Совершенно неожиданным открытием для них, как отмечают авторы работы, стало то, насколько тесно исторические описания постгриппозного истощения во время эпидемии 1889–1890 годов перекликаются с описанием постковидных состояний современными пациентами. Чтение заметок врачей той эпохи почти неотличимо от сегодняшних клинических отчетов, но еще более удивительно, как часто постинфекционными синдромами страдали дети.
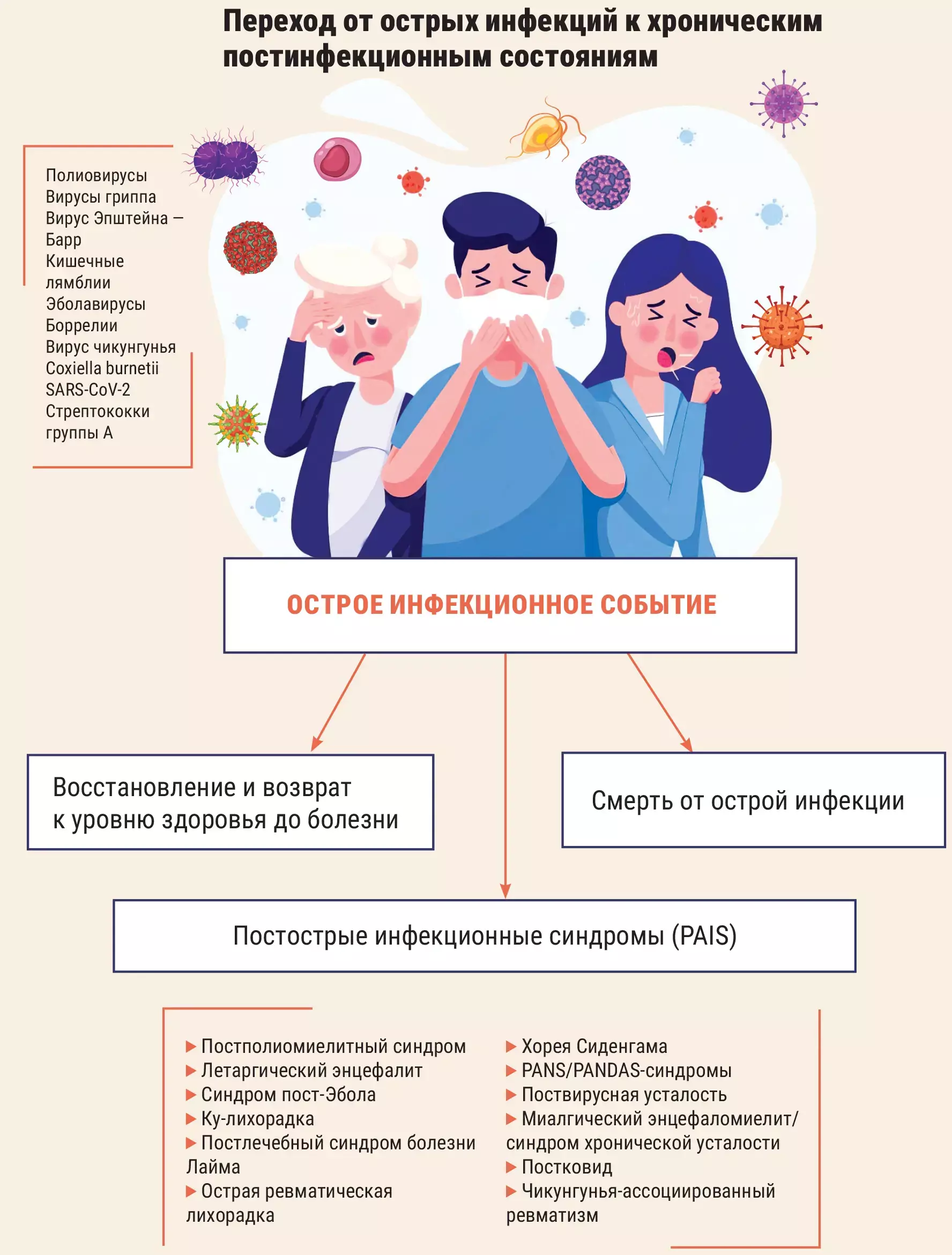
С PAIS ассоциирован широкий спектр патогенов, включая разные классы вирусов, бактерий и паразитов. Конечно, каждый PAIS имеет уникальный триггер и патологию, тем не менее сходства в профилях симптомов и иммунологических находках предполагают, что эти состояния могут иметь общие черты или задействовать пересекающиеся биологические механизмы.
PAIS обладают высокой нагрузкой на здоровье. Но еще хуже то, что пациенты часто сталкиваются со стигмой и недоверием со стороны медиков в ситуациях, когда биомаркеры заболевания неочевидны.
Постинфекционные синдромы в истории эпидемий
Пандемия 1889–1890 годов («русский грипп»)
Предположительно началась в Центральной Азии в мае 1889 года, с первым очагом в Западной Сибири в октябре. К ноябрю и декабрю поразила большую часть Европы и добралась до США, а весной 1890-го — до Азии и Африки.
! Хотя изначально эту эпидемию приписывали вирусу гриппа, современные исследователи предполагают, что причиной мог быть коронавирус OC43; окончательного консенсуса пока нет.
В последующие годы врачи широко сообщали о случаях «постгриппозного истощения» — жалобах на мышечные боли, тревожность, неврит, утомляемость, проблемы со сном и депрессию. Целые тома посвящены документированию этого синдрома, а клинические наблюдения охватывали десятилетия. Термин «постгриппозное истощение» принадлежит врачу Томасу Стрэтчу Даусу, который в публикации 1892 года описал комплекс стойких симптомов и отметил клиническую гетерогенность: у некоторых пациентов симптомы ограничивались одной сферой (например, усталость или невропатия), в то время как у других наблюдалось поражение нескольких систем. В этом же году доктор Дж. Сэмюэл Прайс выступил перед Техасским медицинским советом, подробно описав несколько случаев затяжной реконвалесценции после гриппа с рецидивирующими или стойкими лихорадками, длившимися недели и месяцы.
Пандемия гриппа H1N1 1918–1919 годов («испанка»)
На фоне множества сообщений о постострых стойких неврологических последствиях особенно поразительным явлением стал «летаргический энцефалит», возникающий после перенесенной гриппозной инфекции. Характеризовался широким спектром симптомов, включая энцефалит, кататонию и состояния глубокой летаргии, граничащей с комой. В письме в Canadian Medical Journal в 1932 году доктор Чарльз Хантер описал патологоанатомические находки при аутопсии, отметив «геморрагические очаги в мозге... клеточную инфильтрацию периваскулярных лимфатических оболочек в определенных областях серого вещества, преимущественно состоящую из мелких мононуклеарных лейкоцитов, с заметным отсутствием полиморфноядерных клеток». Хотя пациенты проявляли энцефалопатические симптомы, патология не имела типичных признаков энцефалита, таких как нейтрофильная инфильтрация.
Распространенность была значительной: между 1919 и 1927 годами Министерство здравоохранения Великобритании зарегистрировало 15 935 случаев с предполагаемой летальностью 48 %, 20 % привели к хронической инвалидности и лишь 14 % закончились полным выздоровлением. Только в 1924 году 1 136 школьников в Англии пострадали от этого диагноза, две трети из них никогда полностью не выздоровели.
Лечебные возможности того времени были ограничены, с акцентом на поддерживающие меры. Врачи подчеркивали важность «абсолютного покоя» и давали конкретные диетические рекомендации, включающие молоко, бобы, жирную баранину и жирную свинину.
Одним из самых загадочных аспектов «летаргического энцефалита» является то, что он никогда не наблюдался вне контекста пандемии 1918 года.
Эпидемии полиовируса 1940–1960-х годов
Вспышка 1952 года в США была особенно тяжелой — более 21 тысячи случаев паралитического полиомиелита. Около 75 % случаев проявлялись как легкая гриппоподобная болезнь, однако 25 % прогрессировали до вялого паралича. У ранее инфицированных лиц развивалась прогрессирующая мышечная слабость, глубокая усталость, сильные миалгии и в некоторых случаях рецидивирующий паралич спустя годы или десятилетия после первичной инфекции. Этот комплекс симптомов назван постполиомиелитным синдромом. И хотя впервые он был описан в 1875 году, широкого признания в медицинских и научных кругах не получал до 1980-х годов. Несмотря на десятилетия исследований, основная патобиология остается непонятой.
Вспышка тяжелого острого респираторного синдрома, вызванного SARS, в начале 2000-х годов
Заразилось около 8 тысяч человек с летальностью примерно 10 %. Многие выжившие остались со стойкими инвалидизирующими симптомами после острой фазы, включающими легочные нарушения, мышечную атрофию, нарушения сна, сильную усталость и когнитивные дефициты на протяжении не менее года. Тогда впервые появилось название longSARS, подобно тому, как сейчас отдаленные последствия SARS-CoV-2 называют longCOVID.
Ку-лихорадка в Нидерландах в 2007–2010 годах
После крупнейшей зарегистрированной вспышки этой бактериальной инфекции 10–28 % переболевших сообщали о стойкой усталости, болях, нейрокогнитивных нарушениях, расстройствах сна и респираторных симптомах. Стандартные анализы не показывали ничего необычного, и врачи не могли объяснить причину.
Вспышки Эболы в Западной Африке в 2014–2016 годах
Вирус Эбола, РНК-вирус из семейства Filoviridae, вызывает острую болезнь с лихорадкой, миалгиями, болью в горле и часто прогрессирует до геморрагий, летальность свыше 40 %. Среди выживших многие сообщают о стойких симптомах — усталости, мышечно-скелетных болях, нейрокогнитивных дефицитах и особенно офтальмологических осложнениях. Лонгитюдное иммунофенотипирование выявило устойчивую антивирусную активность, хроническое воспаление и иммунные признаки, напоминающие системную красную волчанку, позволив предположить, что острые вирусные инфекции могут запускать долговременные иммунные изменения, приводящие к хронической дисфункции.
Другие заболевания с «тяжелым хвостом»
Помимо заболеваний с эпидемическим потенциалом еще ряд инфекций вызывают стойкие последствия у некоторых людей.
Вирус Эпштейна — Барр, распространенный герпесвирус, является установленной причиной PAIS.
После инфекционного мононуклеоза у 4–10 % детей и подростков развивается хроническая усталость, длящаяся месяцы или годы.
Пострадавшие испытывают стойкую усталость и рецидивирующие симптомы, напоминающие острую болезнь. Иммунологические исследования выявляют устойчивую активацию Т-клеток и повышенный уровень провоспалительных цитокинов, хотя механизмы остаются неясными. Кроме того, этот вирус теперь считается одним из возможных факторов развития рассеянного склероза.
Болезнь Лайма (боррелиоз) ассоциирована с несколькими хроническими состояниями, включая постлечебный синдром болезни Лайма, развивающийся после антибиотикотерапии при клещевом боррелиозе. Хотя большинство пациентов выздоравливают от острой инфекции при адекватном лечении, 5–10 % сообщают о стойких симптомах, таких как усталость, миалгии, артралгии и невропатические жалобы. Предполагаемые механизмы включают стойкие бактериальные резервуары, не определяемые стандартными культурами из-за подвижности спирохеты, плеоморфизма и иммунного уклонения. Есть и другая теория: остаточные бактериальные компоненты могут поддерживать хроническую иммунную активацию вне активной стадии инфекции.
Вирус чикунгунья, передаваемый комарами и эндемичный для тропических регионов, ассоциирован с хроническим воспалением, напоминающим ревматоидный артрит, в 25 % случаев.
Стрептококковые инфекции группы A хорошо описаны как имеющие постострые последствия. Молекулярная мимикрия между стрептококковыми антигенами и белками хозяина запускает иммуноопосредованную реакцию, поражающую несколько систем органов, приводя к кардитам, артриту, хорее и кожным поражениям. Стрептококк группы A связывают с педиатрическими аутоиммунными нейропсихиатрическими расстройствами (PANDAS), возникающими после перенесенного стрептококкового тонзиллита и характеризующимися внезапным началом тиков, обсессивно-компульсивным поведением (навязчивые мысли), тревожностью и т. д. Как и в случае других PAIS, диагностических биомаркеров нет, что затрудняет распознавание.
Как рождается стигма
Хорошим примером стигматизации постострых инфекционных синдромов являются данные об историческом игнорировании миалгического энцефаломиелита/синдрома хронической усталости, связанного с инфекционными триггерами. Миалгический энцефаломиелит (MЭ) впервые был описан врачом Мелвином Рамси в 1955 году после вспышки необъяснимой болезни среди более 300 сотрудников Королевской больницы в Лондоне. Инфекционный агент так и не был идентифицирован, но болезнь имела много общего с полиомиелитом, включая мышечную слабость, сильную усталость, рецидивирующую лихорадку и неврологические симптомы. Одни пациенты полностью выздоравливали, другие испытывали регулярные рецидивы или болели десятилетиями. О подобных эпидемических вспышках сообщались по всему миру с начала 20-го века, часто в больницах, а спорадические случаи позже выявлялись после разных вирусных инфекций. Соответственно, эти болезни получали разные названия: исландская болезнь, эпидемическая нейромиастения, нейроциркуляторная астения... Доктор Рамси и коллеги предположили, что симптомы могут отражать митохондриальное повреждение, и подчеркивали, что для какого-либо улучшения требуется адекватный отдых.
Хотя MЭ был классифицирован ВОЗ как неврологическое расстройство в 1969 году, болезнь стремительно стигматизировали.
Две статьи 1970 года в British Medical Journal приписали эти вспышки «эпидемической истерии», поскольку в основном они затрагивали женщин-медсестер, а истерия, согласно умонастроениям того времени, типична для «популяций сегрегированных женщин».
В середине 1980-х годов произошли крупные вспышки в США, и исследование выявило структурные аномалии мозга, изменения циркулирующих лимфоцитов и гораздо более частую реактивацию герпесвируса 6-го типа. Тем не менее в 1988 году болезнь была переименована в «синдром хронической усталости» и переопределена Центрами по контролю и профилактике заболеваний, чтобы приуменьшить инфекционное происхождение и сосредоточиться на стойкой, но медицински необъяснимой усталости.
Одна из ведущих гипотез утверждала, что синдром хронической усталости представляет собой мало адаптивную психологическую реакцию на острую инфекцию, при которой больные развивают «отвращение к физической нагрузке, поддерживаемое декондиционированием и неполезными убеждениями о болезни». Широко разрекламированные исследования укрепили представление о синдроме как о психогенной болезни, способствуя распространенному убеждению среди клиницистов и исследователей, что синдром хронической усталости не является отдельной клинической сущностью. В 2015 году появился термин «системная непереносимость нагрузки». В научном сообществе состояние обычно обозначали как миалгический энцефаломиелит/синдром хронической усталости (МЭ/СХУ), были предложены более строгие диагностические критерии, сосредоточенные на кардинальном симптоме постнагрузочного недомогания (PEM), также известного как постнагрузочное нейроиммунное истощение. PEM характеризуется новыми и усиливающимися симптомами после минимальных уровней физической или когнитивной нагрузки, включая гриппоподобные проявления, такие как лихорадка и лимфаденопатия.
Хотя психологические факторы могут играть определенную роль, историческая «психологизация» MЭ/СХУ подчеркивает риски приписывания необъяснимых болезней исключительно психическим причинам.
Синдром хронической усталости признан последствием многих патогенов, включая вирусы Эбола, Эпштейна — Барр, гриппа, SARS-CoV-2 (значительный процент пациентов с постковидом испытывает PEM). Состояние крайне инвалидизирующее: крупный систематический отчет показал, что качество жизни, связанное со здоровьем, ниже в случае MЭ/CХУ, чем при 20 основных заболеваниях, включая рак легких, почечную недостаточность и рассеянный склероз, а долгосрочный уровень выздоровления был определен менее 10 %.
Хотя МЭ/СХУ обычно ассоциируется с инфекционным триггером, он также описан после неинфекционных патологий, таких как сотрясение мозга или черепно-мозговая травма. И это вопрос: способствует ли иммунная дисрегуляция аналогичным образом инфекционно-ассоциированному и неинфекционному синдрому хронической усталости?
P.S. Долгосрочные последствия острых инфекций не являются чем-то новым и не ограничиваются новыми патогенами. Для различных классов микроорганизмов повторяются схожие кластеры симптомов и иммунные паттерны, что подчеркивает: восстановление после инфекции не всегда возвращает здоровье к исходному уровню. Эти исторические и биологические прецеденты дают ключевой контекст для понимания текущих вызовов, связанных с постострыми последствиями современных инфекций, и предлагают ценные сведения о вероятных иммунопатогенных путях, требующих изучения.
