На прошедшей в Минске научно-практической конференции с международным участием «Вызовы современной диагностики. Приоритеты молекулярно-генетической диагностики» выступали не только врачи, ведь тематика предполагает тесное сотрудничество медицинских специалистов и представителей других сфер науки и практики. Директор Института биоорганической химии Национальной академии наук Беларуси, кандидат химических наук, доцент Алексей Янцевич выступил с докладом об исследованиях и разработках в сфере молекулярной диагностики и биоаналитики для медицины.
Биоорганическая химия и медицина
 Алексей ЯнцевичЦель биоорганической химии — изучение взаимосвязи между структурой органических веществ и их биологическими функциями. Эти знания используются для решения практических задач медицины, фармацевтики, сельского хозяйства, химической, пищевой и микробиологической промышленности. Исследуя биополимеры (нуклеиновые кислоты, белки, углеводы), природные малые органические молекулы (липиды, гормоны, антибиотики), синтетические регуляторы (лекарства, пестициды), специалисты решают практические задачи, стоящие перед названными отраслями.
Алексей ЯнцевичЦель биоорганической химии — изучение взаимосвязи между структурой органических веществ и их биологическими функциями. Эти знания используются для решения практических задач медицины, фармацевтики, сельского хозяйства, химической, пищевой и микробиологической промышленности. Исследуя биополимеры (нуклеиновые кислоты, белки, углеводы), природные малые органические молекулы (липиды, гормоны, антибиотики), синтетические регуляторы (лекарства, пестициды), специалисты решают практические задачи, стоящие перед названными отраслями.
Институт проводит фундаментальные и прикладные исследования в области химии, структуры и функции биополимеров и низкомолекулярных биорегуляторов, в том числе белков, нуклеиновых кислот и их компонентов, фосфолипидов, стероидов, простагландинов, брассиностероидов, экдистероидов. Кроме того, в арсенале ученых — разработка и опытно-промышленный выпуск иммунохимических и молекулярно-биологических наборов реактивов для медицинской и ветеринарной диагностики; разработка и производство фармацевтических субстанций, гормональных препаратов и биоспецифических гемосорбентов и др.
С точки зрения биоорганической химии любое заболевание — это, как правило, молекулярная поломка, которая имеет предпосылки (генетические особенности пациента и факторы среды), причину (триггер) и внешние проявления (симптомы). Именно понимание корреляции между структурой и функциями биомолекул позволяет связать между собой все аспекты заболевания.
С позиций фундаментальной науки в основе диагностики всегда находится поиск биомаркеров, то есть показателей, достоверно связанных с развитием и течением заболевания, которые можно объективно измерить.
Диагностика изначально была одним из приоритетных направлений деятельности института. Еще в 1986 году было основано унитарное предприятие «Хозрасчетное опытное производство Института биоорганической химии НАН Беларуси» как специализированное предприятие по производству радиоиммунных наборов для диагностики заболеваний человека. И хотя метод радиоиммунного анализа уходит в историю, развитие новых направлений диагностики с использованием антител продолжается. На сегодняшний день в структуре Института биоорганической химии 12 лабораторий, 7 производственных участков, 1 фармпроизводство. При этом 2 лаборатории выполняют разработки в области молекулярной диагностики и биоаналитики (лаборатория химии белковых гормонов и лаборатория молекулярной диагностики и биотехнологии). А среди научных школ, созданных в Институте, 3 тесно связаны с медициной, в том числе современной молекулярной диагностикой («Молекулярные механизмы монооксигеназного катализа», «Иммуноанализ») и фармацевтикой («Химия компонентов нуклеиновых кислот»).
Мишени и маркеры
Между молекулярной диагностикой и биоаналитикой часто сложно провести границу. Когда мы говорим о молекулярной диагностике, то, как правило, подразумеваем определение последовательности нуклеиновых кислот, что важно для диагностики инфекций, онкологических и наследственных заболеваний, фармакогенетики. Когда говорим о биоаналитике, имеем в виду более широкое понятие, которое включает в себя обнаружение и количественный анализ молекул в образцах биологического происхождения, а это ключ к фармразработке, клинической диагностике, токсикологии, пищевой биоаналитике.
Несмотря на то что генетическая программа развития организма во многом зависит от нуклеиновых кислот, нередко молекулярные поломки происходят на других уровнях и установить особенности развития патологии можно только путем анализа тех молекул, которые, в отличие от ДНК, постоянно изменяются. Речь идет о белках и метаболитах.
Решение многих задач медицины на сегодняшний день сводится к анализу и использованию белковых молекул. В Институте биоорганической химии применяется широкий функциональный спектр молекул и методов работы с ними (см. рис. 1).
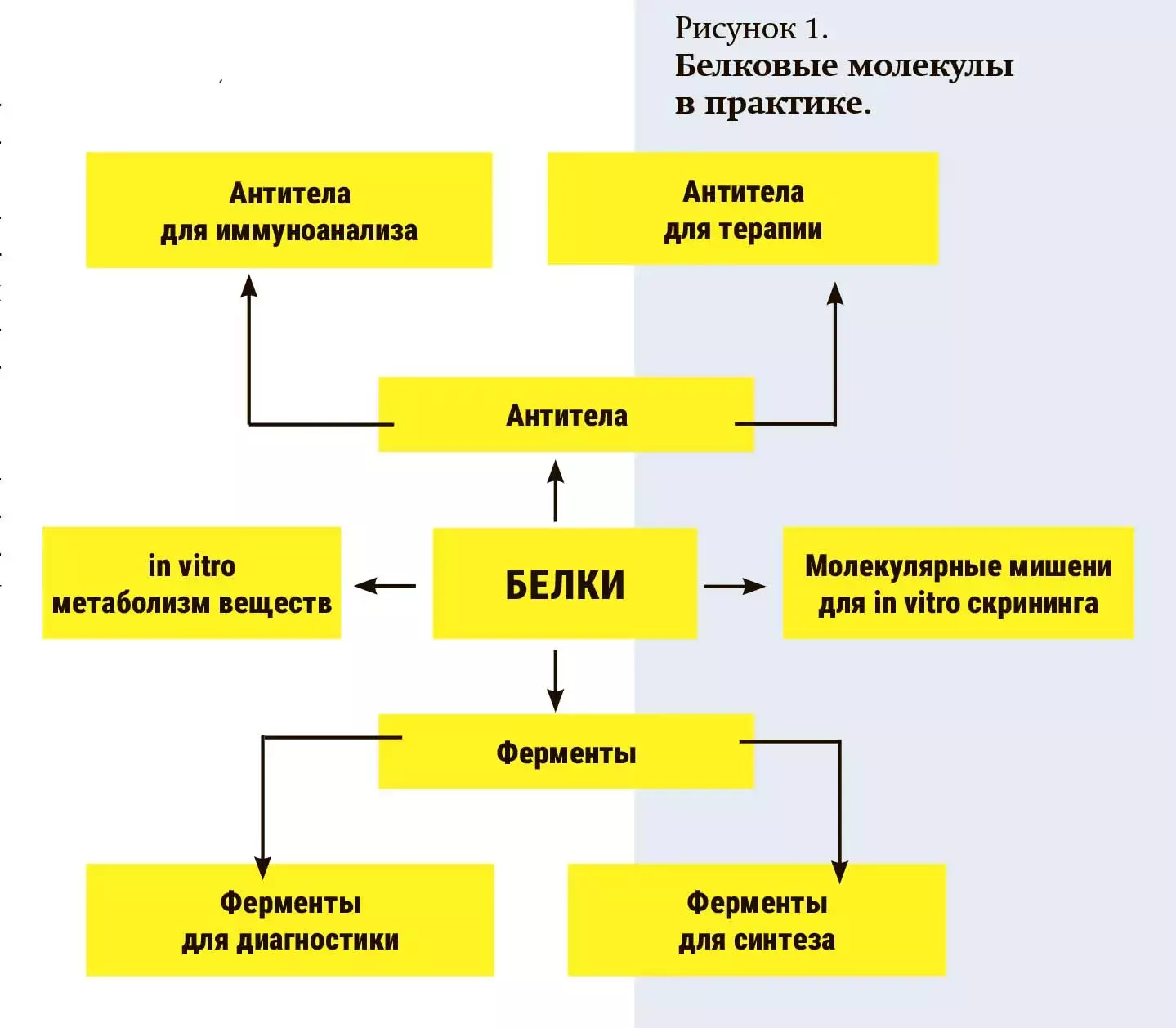
Среди белков, которые важны для диагностики, стоит упомянуть монооксигеназы суперсемейства цитохромов P450 (CYP). Эти ферменты — молекулярные мишени для целого ряда препаратов, среди которых противоопухолевые (ингибиторы ароматазы, в том числе анастрозол и летрозол; ингибиторы 17α-гидроксилазы/17,20-лиазы, в том числе абиратерон), антимикотики (ингибиторы 14α-деметилазы патогенных грибов, в том числе итраконазол, кетоконазол, флуконазол, клотримазол). Представители CYР — фармакогенетические биомаркеры, которые позволяют оценить скорость превращения лекарственных средств в организме пациента (фармакокинетика).
Среди создаваемых в институте молекул для диагностики важны также ДНК-полимеразы, холестерин-оксидазы, антитела, аффинные белковые модули для связывания антибиотиков и нуклеиновых кислот.
ДНК-экзотрансфераза, которую мы рассматриваем как инновационный инструмент для программируемого энзиматического de novo синтеза ДНК, также ключевой компонент набора для детекции апоптоза по методу TUNEL.
Каждый из представителей этих групп молекул ценен как сам по себе в качестве объекта белковой инженерии для создания молекул, обладающих новыми функциями, так и как компонент современных аналитических тест- систем.
Монооксигеназы и фармакогенетика
Монооксигеназы (семейства CYP1, CYP2 и CYP3) играют ключевую роль как фармакогенетические маркеры.
Всего два фермента (CYP2С9 и CYP2С19) участвуют в трансформации около 20 % используемых на сегодня лекарственных соединений.
При этом для каждого фермента описано более 20 полиморфных форм, которые стабильно встречаются в европейской популяции и обладают разной активностью. Соответственно, пациентов разделяют на несколько групп: медленных, стандартных и быстрых метаболизаторов.
Особо важное значение диагностика полиморфных форм имеет для препаратов, у которых очень узкое терапевтическое окно, как у антикоагулянтов, например, варфарина (S-варфарина). Этими же ферментами окисляются нестероидные противовоспалительные препараты (ибупрофен, диклофенак, целекоксиб, пироксикам, индометацин, напроксен), противоэпилептические препараты (фенитоин, вальпроевая кислота), сахароснижающие средства (толбутамид), гипотензивные (лозартан) и противогрибковые (вориконазол) средства, ингибиторы протонной помпы (омепразол), а также некоторые антидепрессанты, определенные антитромбоцитарные средства, кроме того, пропранолол, карбамазепин.
Проблема персонализации фармакотерапии
При внимательном рассмотрении эта проблема может оказаться более глобальной, чем кажется на первый взгляд. Она выходит за границы формулы Парацельса: «Все есть яд и все есть лекарство: одна лишь доза делает яд лекарством, а лекарство ядом», но как нельзя более кратко была сформулирована Александром Суворовым: «Что русскому хорошо, то немцу смерть».
Многие лекарственные препараты высокотоксичны для более чем 10 % населения и не имеют терапевтического эффекта для более чем 15 % людей. Часто развиваются серьезные нежелательные лекарственные реакции.
Эффективность 37 % всех лекарств зависит от генетических особенностей принимающего их человека. По оценке ВОЗ, около 1,5 млн смертельных случаев в год происходят из-за нежелательных реакций (~450 тысяч) и ошибок при приеме лекарств (~1,1 млн).
При одном диагнозе, одном курсе лечения у ряда пациентов лекарство может быть даже вредным — при отсутствии терапевтического эффекта проявляются побочные, в том числе токсические. Таким образом, при назначении любой фармакотерапии всегда необходим анализ активности мишени и активности системы удаления действующего вещества из организма. При этом всегда следует помнить, что эти факторы в свою очередь определяются как генетическими особенностями пациента, что позволяет установить своевременная молекулярная диагностика, так и его образом жизни, стадией заболевания, воздействием окружающей среды, питанием.
Как же правильно назначить лекарство? В идеальном случае для корректной фармакотерапии необходимо организовать одновременно 3 уровня контроля организма: геном, протеом и метаболом. Из этих составляющих наиболее статичен геном. В фармакогенетике нет необходимости знать всю последовательность ДНК пациента, достаточно, как правило, знаний о наличии у него известных, встречающихся в популяции полиморфных форм мишени и ферментов биотрансформации. Это чем-то напоминает информацию о группе крови человека и его резус-факторе: хватает одного анализа в течение жизни, чтобы прогнозировать назначение лекарственных средств. Однако следует помнить, что активность мишеней и ферментов для трансформации зависит также от других факторов, которые проявляются на уровне протеомов и метаболомов. Они связаны с естественным старением организма, особенностями жизни человека, питанием и т. д.
Медикаментозная терапия в психиатрии
Очень остро проблема медикаментозной терапии стоит в ряде направлений медицины. Как правило, в инструкции по применению субстратов полиморфных ферментов и рецепторов включается фармакогенетическая информация. Самое большое количество таких лекарственных средств используется для лечения гематологических и онкозаболеваний, на втором месте находятся психофармацевтические препараты (см. рис. 2).
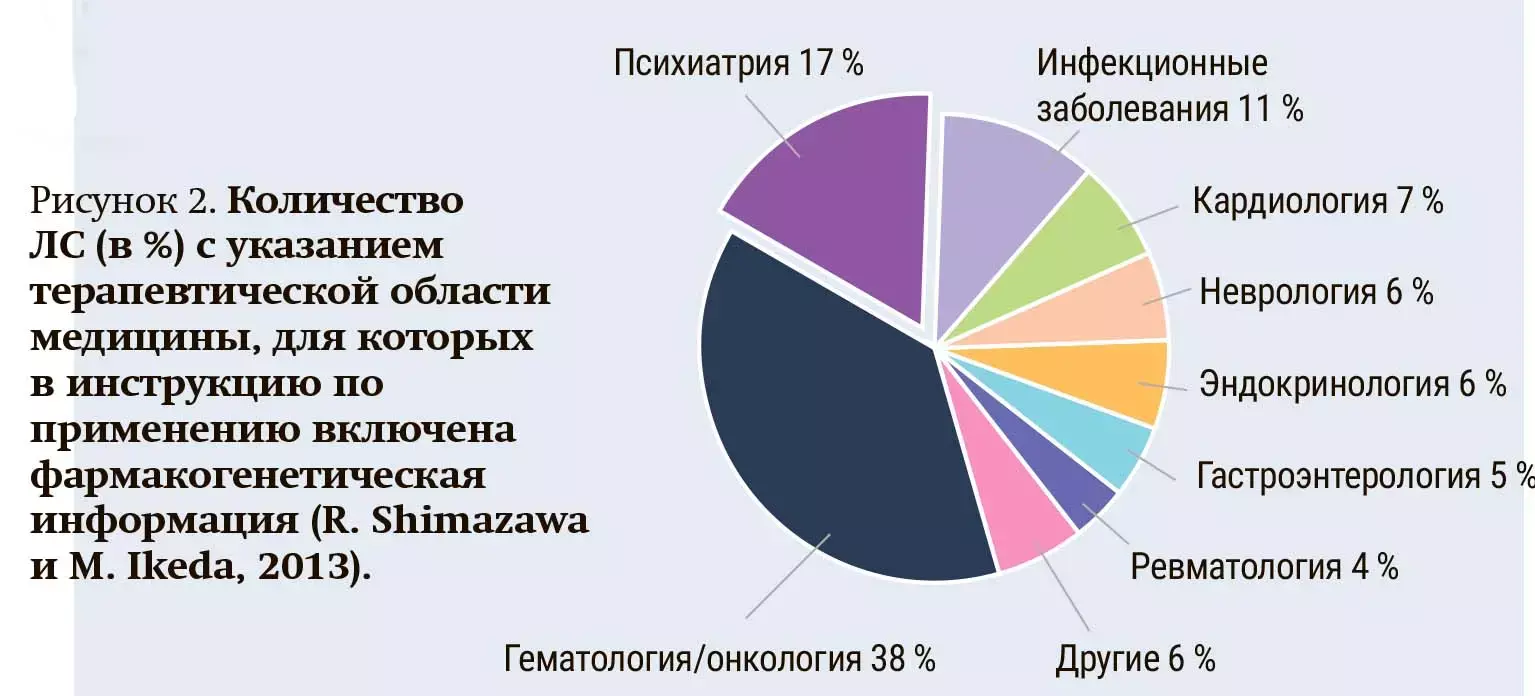
Здесь речь идет не только о том, что препарат может не иметь терапевтического эффекта и время будет потеряно, а о том, что применение некоторых антидепрессантов может привести к появлению суицидального настроения у пациента. Согласно разным оценкам, от 55 % до 70 % пациентов, которые сталкиваются с психофармакологическими препаратами, имеют побочные эффекты, 30–40 % проявляют лекарственную резистентность, когда препарат либо выводится из организма, либо не соответствует мишени.
Сотрудники Института биоорганической химии совместно с работниками РНПЦ психического здоровья провели фармакогенетический анализ с использованием разработанных тестов у более чем 3 тысяч пациентов с шизофренией, эпилепсией, депрессией, тревожными невротическими расстройствами, зависимостями, детским аутизмом. Получен патент «Способ индивидуального подбора лекарственных средств и режима их дозирования при психических и поведенческих расстройствах на основе результатов фармакогенетического тестирования». Разработана, зарегистрирована и внедрена в здравоохранение компьютерная программа «Информационная система для интерпретации результатов фармакогенетического тестирования пациентов при психических и поведенческих расстройствах “Фармакогенетика”», предназначенная для персонализированного подбора терапии психотропными лекарственными средствами.
Другие разработки
За последние десятилетия разработаны наборы для выявления полиморфизма генов CYP2C9/CYP2C19, набор диагностических олигонуклеотидов для определения генетических маркеров фармакорезистентности к психотропным лекарственным средствам, существенное внимание уделено определению генов, связанных с развитием сердечно-сосудистых и эндокринных заболеваний (см. таблицу).
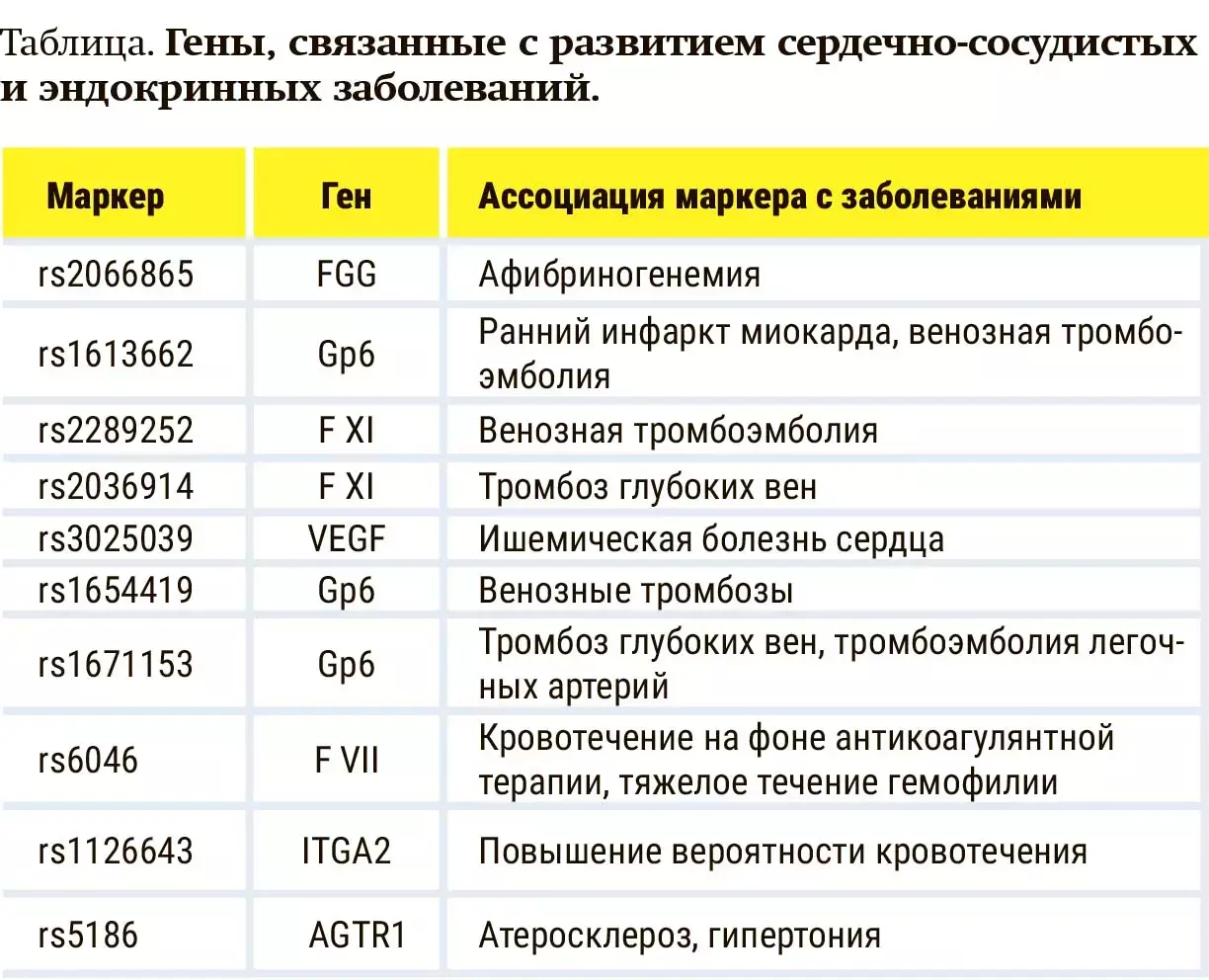
Безопасность пищевых продуктов имеет важнейшее значение для здравоохранения, и в развитии этого направления в Республике Беларусь у Института биоорганической химии серьезный задел. На протяжении многих лет институт разрабатывает и внедряет наборы для пищевой биоаналитики. Это, к примеру, иммуноферментные наборы реагентов ПРОДОСКРИН® для контроля соответствия продуктов питания, пищевого и кормового сырья законодательным стандартам безопасности в части содержания антибиотиков (пенициллинов, тетрациклинов, стрептомицина и др.), микотоксинов (афлатоксин В1, афлатоксин М1 и т. д.).
Внесены тест-системы ПРОДОСКРИН® в перечень стандартов к техническим регламентам Таможенного союза и Евразийского экономического союза ТР ТС 021/2011 «О безопасности пищевой продукции», ТР ТС 033/2013 «О безопасности молока и молочной продукции», ТР ТС 034/2013 «О безопасности мяса и мясной продукции», ТР ЕАЭС 040/2016 «О безопасности рыбы и рыбной продукции».
Стоит упомянуть также о новых молекулярно-генетических методах в пищевой биоаналитике, над которыми сегодня ведется работа. Это в том числе экспресс-тесты (на присутствие в продуктах патогенных бактерий), созданные путем совмещения методов рекомбинантной полимеразной амплификации и иммунохроматографии (мультиплексный экспресс-тест на патогенные бактерии S. enterica, L. monocytogenes, E. coli O157:H7). Схема может быть реализована на одной тест-полоске, когда одновременно можно определять 3 и более патогенов.
Совместно с организациями Министерства здравоохранения разработан метод идентификации патогенных дрожжевых мицелиальных грибов, внедрена соответствующая инструкция по применению.
Перспективы деятельности института до 2030 года определяют такие направления, как работа с нуклеиновыми кислотами (синтез генов, разработка препаратов на основе ДНК) и белками (создание ферментов для in vitro скрининга и поиск новых молекулярных мишеней). Будет продолжена очень важная работа по созданию наборов для тестирования в области пищевой биоаналитики — по выявлению антибиотиков, микотоксинов, патогенов, созданию экспресс-тестов (иммунохроматография), детекции апоптоза. Большое значение для медицины имеет развитие клеточной терапии опухолевых заболеваний (CAR-T), для которой как назначение, так и ход лечения немыслимы без проведения множества диагностических процедур.
В 2026 году началась реализация программы Союзного государства «Союз-Биомембраны» (полное название «Технологическая платформа идентификации новых молекулярных мишеней: мембранных белков и их комплексов»). Это пятилетняя (2026–2030 гг.) научно-техническая инициатива Союзного государства, направленная на создание платформы полного цикла для разработки инновационных лекарств. Программа нацелена на поиск новых молекулярных мишеней, изучение мембранных белков и внедрение терапии для тяжелых заболеваний.
Благодаря современной молекулярной диагностике болезнь можно и нужно предотвратить. Для этого не потребуется слишком много усилий и затрат, нужна систематическая работа по созданию и внедрению средств диагностики.

